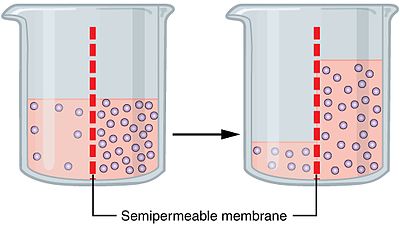
La ósmosis (/ɒzˈmoʊ.sɪs/) es el movimiento neto de moléculas de disolvente (normalmente agua) a través de una membrana semipermeable desde una región de mayor concentración de disolvente (menor concentración de solutos) hacia otra de menor concentración de disolvente (mayor concentración de solutos), sin intervención de una fuerza externa. En español puede pronunciarse /osˈmosis/.
¿Cómo funciona?
La ósmosis se debe al movimiento aleatorio (difusión) de las moléculas de disolvente y a la permeabilidad selectiva de la membrana: la membrana permite el paso del disolvente pero limita o impide el paso de ciertas moléculas de soluto. Como consecuencia, el disolvente tiende a desplazarse hasta equilibrar las concentraciones relativas en ambos lados de la membrana. Cuando no hay balance, se observa un flujo neto de disolvente en una sola dirección.
Es útil distinguir entre ósmosis y difusión: la difusión es el movimiento neto de cualquier especie (soluto o disolvente) por gradiente de concentración, mientras que la ósmosis se refiere específicamente al movimiento del disolvente a través de una membrana semipermeable en presencia de solutos que no atraviesan la membrana.
Presión osmótica
La presión osmótica es la presión externa que debe aplicarse para impedir el movimiento neto de disolvente a través de la membrana. En términos prácticos, se puede considerar como la "fuerza" que ejerce una solución concentrada para atraer solvente. La presión osmótica depende de la concentración de partículas disueltas; en soluciones diluidas puede aproximarse por la ley de Van ’t Hoff:
- π = i M R T
donde π es la presión osmótica, i es el coeficiente de disociación del soluto (número efectivo de partículas por fórmula unitaria), M la concentración molar del soluto, R la constante de los gases y T la temperatura absoluta. En soluciones reales y a altas concentraciones se requieren correcciones.
Tonicidad: efectos sobre las células
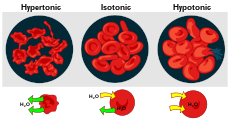
El efecto de una solución sobre una célula depende de la relación entre las concentraciones interiores y exteriores de solutos (tonicidad):
- Solución isotónica: no hay movimiento neto de agua; la célula mantiene su volumen.
- Solución hipotónica (externa): el medio exterior tiene menor concentración de solutos que el interior celular; el agua entra en la célula por ósmosis, pudiendo producir hinchazón y, en células animales, lisis (estallido).
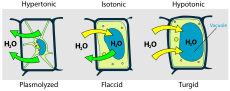
- Solución hipertónica (externa): el medio exterior tiene mayor concentración de solutos; el agua sale de la célula y esta se encoge (plasmólisis en células vegetales, crenación en células animales).
Ósmosis en membranas biológicas
Las membranas celulares son semipermeables: suelen ser impermeables a moléculas grandes como iones cargados, proteínas y polisacáridos, y relativamente permeables a moléculas no polares o pequeñas como gases (O2, CO2), lípidos y ciertos solutos no cargados. La permeabilidad depende de la solubilidad en lípidos, la carga y el tamaño molecular.
El transporte de agua a través de la membrana plasmática puede ocurrir de dos maneras:
- Por difusión simple a través de la bicapa de fosfolípidos.
- Por canales especializados llamados acuaporinas, que facilitan un flujo de agua más rápido y regulado según las necesidades celulares.
Importancia biológica
La ósmosis es crucial en numerosos procesos biológicos:
- Células vegetales: la entrada de agua por ósmosis mantiene la presión de turgencia, que sostiene los tejidos y permite que las plantas permanezcan erguidas. La vacuola central y la pared celular evitan la lisis aun cuando la célula toma gran cantidad de agua.
- Células animales: deben mantener un equilibrio osmótico con su entorno; cambios bruscos de tonicidad pueden dañar las células, por eso organismos multicelulares regulan los fluidos corporales.
- Osmorregulación: organismos como peces, protozoos y bacterias emplean mecanismos (válvulas, bombas iónicas, vacuolas contráctiles) para controlar la entrada y salida de agua y solutos.
- Sistema renal en animales: los riñones usan principios osmóticos para concentrar la orina, reabsorber agua y mantener la homeostasis de electrolitos y volumen sanguíneo.
Aplicaciones tecnológicas y experimentales
La ósmosis tiene aplicaciones prácticas y demostraciones experimentales:
- Ósmosis inversa: proceso usado en desalinización y purificación de agua donde se aplica presión mayor que la presión osmótica para forzar el paso de agua a través de una membrana en sentido contrario, separando el agua pura de los solutos.
- Mediciones de presión osmótica: experimentos con tubos en U y membranas semipermeables permiten medir el flujo de agua y la presión necesaria para detenerlo.
- Medicina: elección de soluciones intravenosas (isotónicas, hipotónicas o hipertónicas) debe considerar los efectos osmóticos sobre las células del paciente.
Riesgos y consideraciones
Un cambio abrupto en la tonicidad del líquido extracelular puede causar choque osmótico, con pérdida de función celular o muerte. Por ello, en medicina y biotecnología es fundamental controlar gradientes osmóticos y la velocidad de cambios en la concentración de solutos.
Resumen
En resumen, la ósmosis es un fenómeno físico-químico fundamental que regula el movimiento de disolvente a través de membranas semipermeables, controla el volumen celular y la presión de turgencia en plantas, y tiene aplicaciones prácticas como la ósmosis inversa y la terapia médica. La presión osmótica y la permeabilidad membranares, incluida la acción de las acuaporinas, determinan la magnitud y dirección del flujo osmótico.