Una pila química convierte la energía química en energía eléctrica. La mayoría de las pilas son células químicas: en el interior de la pila se produce una reacción química que hace que fluya la corriente eléctrica.
¿Qué es una pila y cuáles son sus componentes?
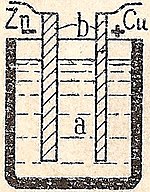
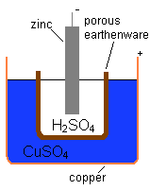
Una pila (o célula electroquímica) es un dispositivo que transforma energía química en energía eléctrica mediante reacciones de oxidación y reducción (redox). Sus componentes principales son:
- Ánodo: electrodo donde ocurre la oxidación (pérdida de electrones).
- Cátodo: electrodo donde ocurre la reducción (ganancia de electrones).
- Electrólito: sustancia conductora iónica que permite el flujo de iones entre ánodo y cátodo.
- Separador: material poroso que evita el contacto directo entre los electrodos pero permite el paso de iones.
Tipos de pilas
Hay dos categorías principales:
- Pilas primarias (no recargables): se usan hasta que las sustancias químicas se agotan y luego se desechan. Ejemplos comunes: alcalinas, zinc-carbono y algunas pilas de litio primarias. Estas pilas suelen ser de «usar y tirar».
- Pilas secundarias (recargables): pueden recargarse haciendo pasar corriente en sentido inverso para revertir las reacciones químicas. Ejemplos: plomo-ácido, NiCd, NiMH, Li-ion y LiPo. Fue Gaston Plante, un científico francés, quien desarrolló las pilas recargables en 1859.
Funcionamiento básico
Cuando se conecta una carga (por ejemplo una lámpara), los electrones fluyen desde el ánodo hacia el cátodo a través del circuito externo. Internamente, el electrólito y los iones se mueven para mantener la neutralidad eléctrica. En una pila recargable se puede invertir el flujo de electrones aplicando corriente desde una fuente externa, lo que restituye los materiales activos y permite un nuevo ciclo de uso.
Características importantes
- Tensión nominal: voltaje típico de una celda (por ejemplo, ~1,5 V para pilas alcalinas AA, ~1,2 V para NiMH, ~3,6–3,7 V para celdas de ion-litio). Las baterías de coche (plomo-ácido) combinan varias celdas para dar ~12 V.
- Capacidad: expresada en miliamperios-hora (mAh) o amperios-hora (Ah); indica cuánta carga eléctrica puede entregar.
- Resistencia interna: afecta la capacidad de entregar corriente y provoca caída de tensión y calentamiento a altas corrientes.
- Autodescarga: pérdida gradual de carga cuando la pila no está en uso; varía según la química (los Li-ion y NiMH tienen autodescarga diferente).
- Ciclos de vida: número de ciclos carga/descarga útiles para pilas recargables antes de que su capacidad disminuya significativamente.
Ejemplos y aplicaciones
- Pilas pequeñas para dispositivos portátiles: mandos, juguetes, cámaras.
- Baterías de iones de litio en teléfonos, ordenadores y vehículos eléctricos.
- Baterías de plomo-ácido en automóviles y sistemas de arranque.
- Sistemas estacionarios y de reserva (UPS), redes y almacenamiento energético con baterías grandes o de flujo.
- Las embarcaciones y los submarinos requieren baterías muy grandes para alimentar motores eléctricos y sistemas a bordo.
Seguridad y medio ambiente
Las pilas contienen materiales que pueden ser peligrosos (ácidos, metales pesados, electrolitos orgánicos). Es importante:
- No abrir ni incinerar pilas.
- Usar cargadores adecuados para pilas recargables (especialmente las de ion-litio, que requieren control de carga CC/CV y protección contra sobrecarga).
- Reciclar o disponer las pilas en puntos autorizados para evitar contaminación y recuperar materiales valiosos.
Consejos prácticos
- Para dispositivos que consumen mucha potencia o se usan habitualmente, conviene usar pilas recargables de buena calidad.
- Al mezclar pilas en un dispositivo, evite combinar nuevas con gastadas o de diferentes químicas, ya que puede producir fugas o mal funcionamiento.
- Almacenar pilas en un lugar seco y fresco para reducir la autodescarga y prolongar su vida útil.
En resumen, las pilas químicas son la tecnología más usada para almacenar y suministrar energía eléctrica de forma portátil. Conocer su funcionamiento, tipos y cuidados ayuda a elegir la opción adecuada según la aplicación y a minimizar riesgos ambientales.