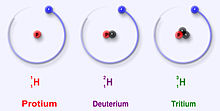
El hidrógeno tiene tres isótopos principales: protio (1H), deuterio (2H) y tritio (3H). Estos isótopos se encuentran de forma natural. El protio y el deuterio son estables; el tritio es radiactivo y tiene una vida media de aproximadamente 12,32 años. Los científicos han creado además otros cuatro isótopos más pesados (H4–H7), pero estos son muy inestables y no existen de forma natural.
¿Qué es un isótopo?
Un isótopo de un elemento químico tiene el mismo número de protones en el núcleo (por eso sigue siendo hidrógeno: 1 protón) pero distinto número de neutrones. Esa diferencia en el número de neutrones produce variaciones en la masa atómica y en algunas propiedades físicas y nucleares, aunque las propiedades químicas sean muy parecidas en muchos casos.
Composición nuclear de los isotopos del hidrógeno
- Protio (1H): 1 protón y 0 neutrones. Es el isótopo más abundante del hidrógeno.
- Deuterio (2H o D): 1 protón y 1 neutrón. Es estable y aproximadamente el 0,015% del hidrógeno natural.
- Tritio (3H o T): 1 protón y 2 neutrones. Es radiactivo, con una vida media de ~12,32 años; se produce en cantidades muy pequeñas de forma natural (por rayos cósmicos) y en reactores nucleares o por reacciones de neutrones.
Abundancia y origen
El protio constituye la gran mayoría del hidrógeno en la Tierra (≈99,98–99,99%). El deuterio aparece en proporciones muy pequeñas (unos 156 partes por millón, ≈0,0156%). El tritio es extremadamente raro en la naturaleza; la mayor parte del tritio existente se genera por procesos artificiales o por interacción de rayos cósmicos con la atmósfera.
Notación y nombres
Además de la notación isotópica con el número de masa (AH), el Unión Internacional de Química Pura y Aplicada (IUPAC) recomienda el uso de 1H, 2H y 3H para identificar los isotopos. Los nombres tradicionales deuterio y tritio y los símbolos abreviados D y T siguen usándose ampliamente en la literatura y en aplicaciones prácticas.
Propiedades y efectos isotópicos
- Las diferencias de masa entre isotopos afectan algunas propiedades físicas: por ejemplo, el agua pesada (D2O) tiene puntos de ebullición y fusión ligeramente mayores que el agua normal (H2O).
- En química y bioquímica existe el efecto isotópico cinético: las reacciones que implican ruptura de enlaces con hidrógeno pueden variar su velocidad si el hidrógeno es deuterio en vez de protio.
- En espectroscopía, el deuterio y el tritio se usan para identificar y rastrear moléculas (marcaje isotópico).
Aplicaciones
- Deuterio: se emplea en forma de agua pesada (D2O) como moderador en algunos reactores nucleares, en experimentos de espectroscopía (NMR), y como trazador en estudios químicos y geológicos.
- Tritio: utilizado en radiomarcadores, en iluminación auto-luminosa (relojes, señales), en investigación como trazador radioactivo y como posible combustible en reacciones de fusión (fusión D–T).
Isótopos inestables H‑4 a H‑7
Los isótopos más pesados del hidrógeno (H4, H5, H6, H7) han sido producidos en experimentos en aceleradores. Son extremadamente inestables y existencias efímeras: decaen casi inmediatamente (medidas en fracciones muy pequeñas de segundo) por emisión de neutrones u otros procesos nucleares, por lo que no se encuentran en la naturaleza de forma estable.
Seguridad y medio ambiente
El tritio, al ser un emisor beta de baja energía, presenta un riesgo externo limitado (la radiación no penetra la piel con facilidad), pero la ingestión, inhalación o absorción puede representar un riesgo radiológico interno. Por ello, su manejo en laboratorios e instalaciones nucleares sigue normas de seguridad específicas para evitar su liberación y exposición.
Resumen: El hidrógeno tiene tres isotopos principales —protio, deuterio y tritio— con propiedades y aplicaciones distintas. Mientras el protio y el deuterio son estables y de uso amplio en ciencia e industria, el tritio es radiactivo y se emplea con precaución en aplicaciones nucleares e investigativas. Otros isotopos más pesados han sido observados en laboratorio pero son altamente inestables.