Cero absoluto: definición, límite térmico y efectos cuánticos
Descubre qué es el cero absoluto, sus límites térmicos y los sorprendentes efectos cuánticos que impiden detener por completo a las partículas.
El cero absoluto es la temperatura a la que las partículas de la materia (moléculas y átomos) se encuentran en sus estados de energía más bajos posibles. No significa, sin embargo, que las partículas "dejen de tener energía" o queden completamente inmóviles en el sentido clásico. En la física cuántica existe la llamada energía de punto cero: incluso si se retira toda la energía térmica, las partículas conservan una energía mínima impuesta por el principio de incertidumbre de Heisenberg. Ese principio establece que cuanto más precisamente se conoce la posición de una partícula, menos precisamente puede conocerse su momento (y viceversa), por lo que no es posible fijar simultáneamente posición y momento con exactitud cero; como consecuencia, una partícula no puede quedar totalmente inmóvil en el sentido clásico.
Acercarse al cero absoluto: técnicas y récords
Los experimentos han conseguido aproximarse extremadamente cerca del cero absoluto. Se han alcanzado temperaturas del orden de 100 pK (cien picokelvin, es decir, 100 × 10−12 K = 10−10 K) por encima del cero absoluto en nubes atómicas muy diluidas. Llegar tan cerca resulta difícil porque cualquier contacto con un cuerpo más caliente introduce calor; además, la radiación ambiental y las vibraciones mecánicas son fuentes de calentamiento. Para enfriar átomos y moléculas se emplean técnicas como el enfriamiento por láseres (laser cooling), el enfriamiento evaporativo en trampas magnéticas u ópticas, la desmagnetización adiabática y refrigeradores de dilución, entre otras.
Escalas de temperatura
Las escalas de temperatura kelvin y Rankine se definen de manera que el cero absoluto es 0 kelvin (K) o 0 grados Rankine (°R). En las escalas Celsius y Fahrenheit el cero absoluto corresponde a -273,15 °C o -459,67 °F, respectivamente —es decir, son conversiones lineales entre escalas.
Comportamiento físico cerca del cero absoluto
Al disminuir la temperatura hacia cero, la energía térmica de las partículas se reduce y muchas propiedades macroscópicas cambian de forma notable. Para un gas ideal, la presión tiende a cero cuando la temperatura tiende a cero porque la presión depende del movimiento térmico de las partículas. Sin embargo, en sólidos y en sistemas con interacciones fuertes la situación es más compleja: existen fuerzas internas, estados ligados y efectos de interacción que impiden concluir de forma general que la "presión sea cero".
En los sólidos, la energía térmica se manifiesta como excitaciones colectivas (fonones) que describen las vibraciones de la red cristalina. Al acercarse al cero absoluto, la amplitud de estas vibraciones térmicas disminuye, pero permanece la energía de punto cero asociada a los modos cuánticos. La idea de "vibrar en sentido inverso" no aplica como una forma de compensación para anular totalmente el movimiento: el movimiento térmico se reduce pero no se invierte para crear movimiento negativo que suprima toda vibración.
En cuanto a la conducción eléctrica, muchos metales reducen su resistividad al bajar la temperatura; además, ciertos materiales experimentan una transición a un estado superconductivo por debajo de una temperatura crítica, en el que la resistencia eléctrica cae a cero y se presentan fenómenos macroscópicos cuánticos (corrientes persistentes, efecto Meissner). No todos los materiales se convierten en superconductores, y la superconductividad aparece únicamente bajo condiciones particulares.
Leyes de la termodinámica y el cero absoluto
La TerceraLey de la Termodinámica se puede formular de dos maneras complementarias: una versión (el teorema de Nernst) indica que la entropía de un sistema perfecto tiende a una constante (a menudo cero) cuando T → 0; otra versión, llamada principio de inaccesibilidad, establece que es imposible alcanzar el cero absoluto mediante un número finito de procesos físicos. En la práctica, esto significa que aunque podamos aproximarnos arbitrariamente cerca, no podemos lograr exactamente 0 K con procedimientos finitos.
La Segunda Ley de la Termodinámica implica límites en la eficiencia de las máquinas térmicas. Para un ciclo reversible ideal (ciclo de Carnot) la eficiencia máxima viene dada por η = 1 − Tfría/Tcaliente. En las frases originales se emplearon las expresiones "temperatura exterior" y "temperatura interior"; la idea es la misma: la eficiencia solo alcanzaría el 100% si la temperatura del foco frío fuera 0 K, lo cual no es alcanzable. Por eso ningún motor térmico puede ser 100% eficiente en la práctica; sin embargo, su eficiencia puede acercarse más a 1 aumentando la temperatura del foco caliente y/o reduciendo la del foco frío.
Efectos cuánticos y aplicaciones
A temperaturas cercanas al cero absoluto aparecen y se estudian numerosos fenómenos cuánticos macroscopios: condensados de Bose-Einstein, superfluidez, superconductividad, correlaciones cuánticas y estados cuánticos coherentes con aplicaciones en relojes atómicos, sensores de alta precisión y computación cuántica. Los sistemas ultra-fríos constituyen laboratorios ideales para estudiar física fundamental, interacciones cuánticas y simulaciones de modelos teóricos.
Notas finales
- La energía térmica tiende a desaparecer al bajar la temperatura, pero la energía de punto cero y otros efectos cuánticos persisten.
- El comportamiento macroscópico (presión, resistencia eléctrica, calor específico) depende del tipo de materia y de interacciones; no existe una única respuesta universal válida para todos los materiales.
- Las técnicas experimentales para alcanzar temperaturas ultra-bajas combinan métodos ópticos, magnéticos y criogénicos; la investigación en este campo sigue avanzando y ampliando nuestras capacidades para explorar regímenes cuánticos extremos.
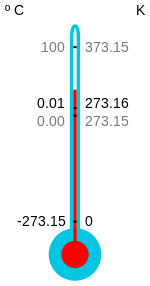
El cero kelvin (-273,15 °C) se define como el cero absoluto.
Páginas relacionadas
- Temperatura absoluta
- Calor absoluto
Preguntas y respuestas
P: ¿Qué es el cero absoluto?
R: El cero absoluto es la temperatura a la que las partículas de la materia (moléculas y átomos) se encuentran en sus puntos de energía más bajos.
P: ¿Significa el cero absoluto que las partículas pierden toda su energía y dejan de moverse?
R: No, en física cuántica existe algo llamado energía de punto cero, que significa que incluso después de haber eliminado toda la energía de las partículas, éstas siguen teniendo algo de energía debido al principio de incertidumbre de Heisenberg.
P: ¿Cuál es la temperatura récord alcanzada cerca del cero absoluto?
R: La temperatura récord fue de 100 pK (cien picokelvin, igual a 10-10 kelvin) por encima del cero absoluto.
P: ¿Cómo enfrían los científicos los objetos a temperaturas muy bajas?
R: Los científicos utilizan láseres para frenar los átomos cuando enfrían objetos a temperaturas muy bajas.
P: ¿Cómo se definen las escalas Celsius y Fahrenheit con respecto al cero absoluto?
R: Las escalas Celsius y Fahrenheit están definidas de forma que el cero absoluto es -273,15°C o -459,67°F.
P: ¿Qué dice la Tercera Ley de la Termodinámica sobre el cero absoluto?
R: La Tercera Ley de la Termodinámica dice que nada puede tener nunca una temperatura de cero absoluto.
P: ¿Cómo se puede aumentar la eficiencia de un motor para acercarse al 100%?
R: La eficiencia de un motor se puede aumentar más cerca del 100% haciendo que la temperatura interior sea más caliente y/o la temperatura exterior más fría, de acuerdo con la Segunda Ley de la Termodinámica.
Buscar dentro de la enciclopedia