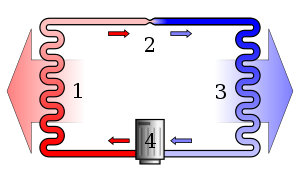
La segunda ley de la termodinámica establece que, cuando la energía cambia de una forma a otra o la materia se redistribuye libremente, la entropía (una medida del desorden o, más precisamente, de la dispersión de energía) de un sistema aislado tiende a aumentar. En términos prácticos esto significa que los procesos espontáneos ocurren en la dirección que incrementa la dispersión de energía entre los estados accesibles del sistema.
Gradientes y equilibrio
Las diferencias de temperatura, presión y densidad tienden a igualarse con el tiempo por difusión, conducción y convección; es decir, la energía y la materia se redistribuyen hasta alcanzar el equilibrio termodinámico. Sin embargo, en presencia de campos externos (por ejemplo, la gravedad) algunas cantidades no se igualan «horizontalmente»: la gravedad impone una variación vertical en la presión y la densidad. Por eso, en equilibrio hidrostático la densidad y la presión en la parte inferior serán mayores que en la parte superior.
¿Qué es la entropía?
La entropía puede entenderse como una medida de la dispersión de energía y de la cantidad de microestados (configuraciones microscópicas) compatibles con un mismo estado macroscópico. Cuanto más se puede "esparcir" la energía entre partículas y modos, mayor es la entropía. La entropía tiene unidades de energía dividida por temperatura (J/K).
En procesos espontáneos la energía útil disponible para realizar trabajo tiende a disminuir porque se distribuye en formas menos aprovechables (por ejemplo, calor a baja temperatura). No obstante, localmente puede disminuir la entropía (por ejemplo, en sistemas vivientes) siempre que el entorno compense ese descenso con un aumento mayor de entropía total.
Enunciados clásicos
La formulación más conocida de la segunda ley se atribuye a Rudolf Clausius:
El calor no puede pasar por sí mismo de un cuerpo más frío a otro más caliente.
Otra declaración equivalente, dada por Lord Kelvin, es:
Una transformación cuyo único resultado final es convertir el calor, extraído de una fuente a temperatura constante, en trabajo, es imposible.
Estos enunciados enfatizan que existen límites en la conversión completa de calor en trabajo y que el calor tiende a fluir de zonas calientes a frías, no al revés, sin intervención externa.
Formulación matemática
Para un sistema aislado la segunda ley puede expresarse como:
- ΔS_total ≥ 0, donde ΔS_total es la variación de la entropía del sistema aislado.
- Para procesos reversibles: ΔS = 0. Para procesos irreversibles: ΔS > 0.
- Para un proceso que intercambia calor con un entorno a temperatura T, en un proceso reversible diferencial: dS = δQ_rev / T. En general, dS ≥ δQ / T, y la generación de entropía interna S_gen satisface S_gen ≥ 0.
Interpretación estadística
Desde la termodinámica estadística, propuesta por Boltzmann y otros, la entropía S se relaciona con el número de microestados W compatibles con un macroestado por la expresión:
S = k ln W, donde k es la constante de Boltzmann (≈ 1.38·10^-23 J/K).
Esta formulación explica por qué la segunda ley es una ley de probabilidad: los estados con mayor número de microconfiguraciones son mucho más probables, de modo que los sistemas evolucionan hacia ellos con gran probabilidad cuando no hay restricciones externas.
Ejemplos y aplicaciones
- Transferencia de calor: dos cuerpos a distinta temperatura alcanzan una única temperatura de equilibrio; la entropía total aumenta.
- Mezcla de gases: dos gases inicialmente separados se mezclan espontáneamente; la entropía aumenta porque hay más microestados posibles.
- Expansión libre de un gas: el gas ocupa más volumen y su entropía aumenta.
- Fricción: convierte energía mecánica ordenada en calor disperso, generando entropía.
- Motores térmicos: la eficiencia máxima de un motor que trabaja entre dos depósitos térmicos viene dada por el ciclo de Carnot y está limitada por 1 − T_fría/T_caliente; esto deriva directamente de la segunda ley.
Limitaciones, fluctuaciones y detalles
La segunda ley describe el comportamiento probable de sistemas con muchos grados de libertad. En sistemas muy pequeños o en tiempos muy cortos pueden producirse fluctuaciones que momentáneamente disminuyan la entropía local; esto está contemplado en teoremas de fluctuación y en la física estadística moderna. Sin embargo, en sistemas macroscópicos estas fluctuaciones son extraordinariamente improbables y la ley se cumple con enorme certeza.
Además, la ley se aplica estrictamente a sistemas aislados: en sistemas abiertos es posible una disminución local de entropía si hay intercambio de energía y materia con el entorno que compense esa disminución.
Problemas conceptuales históricos, como el demonio de Maxwell, se resolvieron entendiendo el papel de la información y del coste energético asociado a las operaciones que realiza el demonio: mantener o reducir el desorden requiere, en última instancia, un aumento neto de entropía en el universo.
Consecuencias conceptuales
La segunda ley introduce una dirección preferente en los procesos naturales: la llamada "flecha del tiempo" termodinámica. Mientras otras leyes microscopicas son reversibles, la segunda ley explica por qué las evoluciones macroscópicas espontáneas tienen una dirección temporal preferida hacia estados de mayor dispersión de energía.
En resumen: la segunda ley de la termodinámica limita las transformaciones de energía, define la direccionalidad de los procesos naturales y puede ser entendida tanto de forma macroscópica (Clausius, Kelvin) como estadística (Boltzmann). Su validez práctica es enorme en ingeniería, física, química y biología, aunque su formulación probabilística admite excepciones temporales y locales en sistemas pequeños o fuertemente fluctuantes.