En química, las fuerzas de Van der Waals son un tipo de fuerza intermolecular. Una fuerza intermolecular es una fuerza relativamente débil que mantiene unidas a las moléculas. Las fuerzas de Van der Waals son el tipo más débil de fuerza intermolecular. Deben su nombre al científico holandés Johannes Diderik van der Waals (1837-1923).
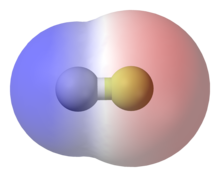
Los electrones con carga negativa orbitan alrededor de las moléculas o los iones. Los electrones crean cargas ligeramente diferentes de un extremo a otro de la molécula. Estas ligeras diferencias se denominan cargas parciales, como δ - o δ +.
El término se utiliza a veces de forma imprecisa como sinónimo de todas las fuerzas intermoleculares. Las fuerzas de Van der Waals son relativamente débiles en comparación con los enlaces covalentes, pero desempeñan un papel fundamental en la química supramolecular, las enzimas, la ciencia de los polímeros, la nanotecnología, la ciencia de las superficies y la física de la materia condensada. Las fuerzas de Van der Waals definen muchas propiedades de los compuestos orgánicos, incluida su solubilidad.
Tipos principales de fuerzas de Van der Waals
- Fuerzas de dispersión de London (inducidas por fluctuaciones cuánticas): Son debidas a variaciones instantáneas en la distribución electrónica que crean dipolos temporales. Afectan a todas las moléculas, incluso a las no polares, y son responsables, por ejemplo, de que los gases nobles puedan licuarse a baja temperatura.
- Interacciones dipolo–dipolo (Keesom): Ocurren entre moléculas con dipolos permanentes (moléculas polares); las orientaciones favorables de los dipolos producen atracción electrostática.
- Interacciones dipolo–dipolo inducido (Debye): Un dipolo permanente puede inducir un dipolo temporal en una molécula vecina no polar, provocando atracción.
- Puentes de hidrógeno (a menudo considerados aparte): Aunque muchas veces se clasifican como una categoría distinta dado su mayor carácter direccional y energía (por ejemplo, O–H···O, N–H···O), en contextos generales se mencionan junto a las fuerzas intermoleculares y son cruciales en estructuras biológicas.
Características físicas y dependencia de la distancia
Las fuerzas de Van der Waals son de corto alcance y su intensidad cae rápidamente con la distancia entre moléculas. La contribución dominante de dispersión tiene una dependencia aproximada con la distancia r proporcional a r-6 (atracción) en el régimen intermolecular. En modelos empíricos como el potencial de Lennard-Jones se representa así: V(r) = 4ε[(σ/r)12 − (σ/r)6], donde el término r-12 representa la repulsión muy fuerte a distancias muy pequeñas y r-6 la atracción de Van der Waals.
Factores que influyen en la magnitud
- Polarizabilidad: Moléculas grandes o con electrones más desplazables presentan fuerzas de dispersión más fuertes.
- Tamaño y forma molecular: Mayor área de contacto favorece interacciones; las cadenas largas de hidrocarburos muestran mayores fuerzas de Van der Waals entre sí que moléculas compactas.
- Polaridad: Moléculas polares experimentan interacciones dipolo–dipolo además de dispersión.
- Temperatura: A temperaturas más altas la energía térmica puede vencer a estas fuerzas, reduciendo su efecto macroscópico (por ejemplo, disminuye la viscosidad relativa, facilita evaporación).
- Presencia de grupos funcionales: Grupos capaces de formar puentes de hidrógeno o interacciones específicas modifican notablemente la interacción total entre moléculas.
Ejemplos y aplicaciones
- Liquefacción de gases nobles (He, Ne, Ar): debida exclusivamente a fuerzas de dispersión.
- Tendencias en puntos de ebullición de los alcanos: aumentan con la masa y la superficie molecular por mayor dispersión.
- Adhesión y fricción a escala nanométrica: las fuerzas de Van der Waals explican por qué materiales como el grafeno o ciertos adhesivos secos funcionan a escala microscópica.
- Gecko: los pies de los gecos se adhieren a superficies por interacciones Van der Waals entre millones de microsetas y la superficie.
- Estructura y plegamiento de proteínas, apilamiento de bases en el ADN (interacciones π–π), autoensamblaje de moléculas y eficiencia en catálisis y reconocimiento molecular.
Modelos, medición y términos relacionados
Además del potencial de Lennard-Jones, las interacciones de Van der Waals se tratan mediante la teoría de perturbaciones de la polarizabilidad y métodos cuánticos que permiten calcular la energía de dispersión (por ejemplo, correcciones DFT-D en química computacional). En la práctica experimental se investigan con técnicas como microscopia de fuerzas (AFM), espectroscopía y medidas de tensión superficial o fuerzas entre superficies con aparatos de fuerza superficial.
También aparecen conceptos útiles como el radio de Van der Waals (una medida de tamaño efectivo de un átomo/molécula en reposo) y la energía de cohesión en sólidos moleculares, que depende en gran parte de estas fuerzas.
Importancia en química y ciencias afines
Aunque son débiles comparadas con los enlaces covalentes o iónicos, las fuerzas de Van der Waals gobiernan muchos fenómenos colectivos y propiedades físicas: puntos de fusión y ebullición, solubilidad, estabilidad de fases, y el comportamiento en interfaces. En biología molecular definen interacciones de reconocimiento entre biomoléculas y en nanotecnología condicionan la manipulación y ensamblaje de nanoestructuras.
En resumen, las fuerzas de Van der Waals —si bien pequeñas a escala de una sola interacción— sumadas a gran número determinan comportamientos macroscópicos y son esenciales para entender y diseñar materiales, procesos y sistemas a escalas desde molecular hasta macroscópica.

