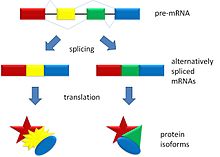
El splicing alternativo es un proceso mediante el cual un mismo gen puede dar lugar a varios ARN mensajeros maduros diferentes y, por tanto, a proteínas distintas. Este mecanismo modifica la composición de los exones incluidos en el producto final después del procesamiento del ARN pre-mensajero, aumentando la diversidad funcional del genoma sin necesidad de aumentar el número de genes.
¿Qué es y por qué importa?
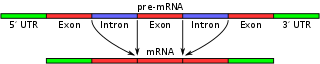
Durante la transcripción se sintetiza un ARN precursor que contiene exones (regiones codificantes o no codificantes que se mantienen en el ARNm) e intrones (regiones que suelen eliminarse). En el empalme alternativo, esos exones y partes de intrones se reconectan de distintas formas, generando diferentes isoformas de ARNm a partir del mismo gen. En los eucariotas esto es muy frecuente: en humanos ~95% de los genes con múltiples exones experimentan empalme alternativo, lo que contribuye en gran medida a la complejidad proteica y funcional de los tejidos y órganos.
Mecanismos y elementos moleculares
El empalme lo lleva a cabo el spliceosoma, un complejo ribonucleoproteico que reconoce señales en el ARN precursor:
- Sitio de empalme 5' (donor) y 3' (acceptor).
- Punto de rama y la región rica en pirimidinas aguas arriba del sitio 3'.
- Elementos reguladores cis: ESE (enhancers de exón), ESS (silencers de exón), ISE e ISS (elementos intrónicos).
- Factores trans: proteínas como las familias SR (activadores del empalme) y hnRNP (generalmente represores) que se unen a esos elementos cis y modulan la selección de sitios de empalme.
La combinación de estas señales y proteínas determina qué sitios son utilizados en cada célula o en respuesta a estímulos, y cambios en estas interacciones alteran el patrón de empalme.
Tipos principales de splicing alternativo
Entre los patrones más comunes de empalme alternativo se incluyen:
- Omisión o salto de exón (exon skipping): un exón se incluye en algunos ARNm y se omite en otros.
- Uso alternativo de sitios 5' o 3': selección de diferentes puntos de inicio o fin de un exón, cambiando el marco de lectura o la secuencia proteica.
- Exones mutuamente exclusivos: dos exones nunca se incluyen simultáneamente; solo uno aparece por ARNm.
- Retención de intrón: un intrón no se elimina y queda en el ARNm maduro; puede alterar la traducción o ocasionar degradación.
- Promotores alternativos y poliadenilación alternativa: cambios en el inicio de la transcripción o en el sitio de poliadenilación que producen isoformas con diferentes UTRs y regulación.
Regulación espacial y temporal
El empalme alternativo es regulado de forma específica por tejido, etapa del desarrollo, señales ambientales y estado fisiológico. Por ejemplo, determinados factores de empalme están expresados preferentemente en el sistema nervioso y promueven isoformas neuronales; otros factores responden a señales hormonales o al estrés celular. Cambios en la concentración o actividad de proteínas reguladoras (modificaciones postraduccionales como fosforilación) alteran los patrones de empalme.
Consecuencias funcionales
Las isoformas generadas por empalme alternativo pueden diferir en:
- Actividad enzimática o capacidad de interacción con otras proteínas.
- Localización subcelular (por inclusión/omisión de señales de localización).
- Estabilidad del ARNm (UTRs distintas) y de la proteína.
- Presencia de sitios de regulación por microARNs.
Algunas isoformas pueden ser no funcionales o incluso dominantes negativas; otras expanden la capacidad funcional de una familia proteica.
Relevancia clínica: enfermedades y terapias
Variantes que alteran sitios de empalme o la regulación del empalme causan o contribuyen a numerosas enfermedades genéticas y al cáncer. Por ejemplo:
- La exclusión del exón 7 del gen SMN2 es central en la atrofia muscular espinal (SMA).
- Mutaciones que crean o destruyen sitios de empalme en genes tumorales pueden favorecer oncogénesis.
Existen estrategias terapéuticas dirigidas al empalme:
- Oligonucleótidos antisentido (ASOs) o splicing-switching oligonucleotides diseñados para modificar la unión de factores y restaurar un patrón de empalme correcto (ej. nusinersen para SMA).
- Pequeñas moléculas que modulan la actividad de factores del empalme.
- Terapias génicas y edición del genoma para corregir variantes de empalme.
Mecanismos de control de calidad
Isoformas aberrantes que contienen codones de terminación prematuros suelen ser reconocidas y eliminadas por vías de control de calidad del ARNm, destacando la degradación mediada por cadenas con terminación prematura (NMD, nonsense-mediated decay). Proteínas mal plegadas o truncadas resultantes de empalme defectuoso pueden ser degradadas por sistemas proteolíticos. En el texto original se indicaba que los productos no funcionales «son desmenuzados por enzimas»; en términos moleculares esto incluye nucleasas, complejo exosoma y proteasas, entre otros sistemas enzimáticos responsables de la eliminación de materiales defectuosos.
Detección y análisis
Los patrones de empalme se analizan experimentalmente mediante:
- RT‑PCR y PCR semicuantitativa para isoformas conocidas.
- Secuenciación masiva de ARN (RNA‑seq) para identificar y cuantificar isoformas a escala genómica.
- Microarrays específicos y ensayos funcionales de unión proteína‑ARN.
El análisis bioinformático detecta variantes de empalme, cuantifica abundancias y predice impactos funcionales.
Importancia evolutiva
El splicing alternativo permite a los organismos aumentar la complejidad proteica sin duplicar genes, facilitando la evolución de funciones nuevas y la especialización tisular. Cambios en patrones de empalme han sido una fuente importante de diversidad proteómica en eucariotas.
Resumen
El splicing alternativo es un proceso esencial en eucariotas que expande la diversidad funcional del genoma al generar múltiples ARN y proteínas a partir de un solo gen. Su regulación fina —mediada por señales en el ARN y por proteínas reguladoras— es clave para el desarrollo, la homeostasis y la adaptación; su desregulación está implicada en numerosas enfermedades, pero también ofrece dianas terapéuticas concretas.