Encendedor de Döbereiner: primer mechero químico a base de hidrógeno (1823)
Encendedor de Döbereiner (1823): primer mechero químico a hidrógeno. Descubre su historia, la reacción Zn+H₂SO₄, el papel del platino y su funcionamiento pionero en química.
La lámpara de Döbereiner es uno de los primeros encendedores prácticos. Fue desarrollada en 1823 por el químico alemán Johann Wolfgang Döbereiner y se fabricó comercialmente hasta aproximadamente 1880. Era apreciada como un encendedor fiable y “sin chispa” para encender pipas, cigarros y velas en hogares y gabinetes científicos. El Castillo de Heidelberg y también el Deutsches Museum (Museo Alemán) conservan lámparas originales de Döbereiner para mostrarlas y documentar su importancia histórica.
Funcionamiento básico
El encendedor funciona aprovechando una reacción química que produce hidrógeno, y la posterior combustión de ese hidrógeno con el oxígeno del aire. En el interior del mecanismo hay una botella o recipiente de vidrio (a en la imagen de la derecha) que contiene ácido sulfúrico. En otra cámara abierta (botella (b)) se coloca zinc. En la parte superior hay una válvula que puede abrirse y cerrarse con una palanca (f).
Reacciones químicas
Al accionar la palanca se abre la conexión entre el depósito de ácido y la cámara del zinc; el ácido fluye hacia el zinc y comienza la reacción ácido–metal, que libera hidrógeno:
Z n + H 2 S O 4 ⟶ Z n 2 + + S O 4 2 - + H 2 ↑ {\displaystyle \mathrm {Zn+H_{2}SO_{4}\longrightarrow Zn^{2+}+SO_{4}^2-}+H_{2}uparrow } }
El hidrógeno generado sale por la parte superior del aparato y debe pasar por una pequeña esponja o lámina de platino situada junto a la válvula. El platino actúa como catalizador: facilita la recombinación del hidrógeno con el oxígeno del aire sin consumirse y libera suficiente energía para que la mezcla de gases (oxihidrógeno) arda espontáneamente formando vapor de agua:
2 H 2 + O 2 ⟶ 2 H 2 O {\displaystyle \mathrm {2\ H_{2}+O_{2}\longrightarrow 2\ H_{2}O} } }
Partes y diseño
- Depósito de ácido sulfúrico: recipiente que almacena el ácido concentrado.
- Cámara del zinc: donde se coloca el metal que reacciona con el ácido.
- Palanca y válvula: mecanismos mecánicos que permiten el paso controlado del ácido al zinc y la salida del gas.
- Elemento de platino: pequeña porción de platino (a veces en forma de esponja o alambre enrollado) que actúa como catalizador y punto de ignición.
- Cuerpo de vidrio y cierres: elementos constructivos que mantienen separadas las fases líquida y gaseosa y permiten el cierre para detener la reacción.
Operación y control
El encendedor se pone en marcha accionando la palanca. Cuando se suelta de nuevo (cerrando la válvula), el ácido deja de alcanzar el zinc, la producción de hidrógeno cesa y el gas restante en la cámara no puede escapar, de modo que la presión empuja el ácido de vuelta al depósito de vidrio; así se detiene la llama. Este diseño permitía un control razonable de la generación de gas y del encendido.
Ventajas, inconvenientes y seguridad
- Ventajas: encendido fiable y sin chispa, rapidez en obtener una llama, mecanismo ingenioso desde el punto de vista químico y tecnológico.
- Inconvenientes: uso de ácido sulfúrico corrosivo, necesidad de manipular zinc y hidrógeno (gas inflamable), y el coste del platino como componente catalítico. Además, no eran tan portátiles ni seguros como los encendedores posteriores.
- Riesgos: quemaduras por ácido, fugas de hidrógeno que pueden crear atmósferas explosivas si no se ventilan correctamente y corrosión de partes metálicas. Por ello su uso requiere precaución y mantenimiento adecuado.
Difusión y declive
La lámpara de Döbereiner fue popular en la primera mitad del siglo XIX y fabricada hasta finales de ese siglo, pero fue quedando obsoleta con la aparición de medios más seguros y baratos para encender fuego: primero las cerillas de fricción y, más tarde, los encendedores modernos. La necesidad de manejar ácido y el precio del platino limitaron su uso doméstico generalizado.
Conservación y valor histórico
Hoy las lámparas de Döbereiner se conservan como piezas de historia de la química y de la tecnología. Además del Castillo de Heidelberg y del Deutsches Museum, otros museos de ciencia y colecciones privadas muestran ejemplares que ilustran la relación entre la investigación química y los primeros dispositivos prácticos para la vida cotidiana. Son objetos valiosos tanto por su diseño como por su significado en la historia de la química aplicable.

La lámpara de Döbereiner.
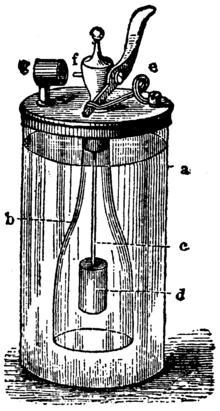
Lámpara de Döbereiner: a. cilindro de vidriob . botella abiertac. cableado . zince . llave de pasof . boquillaleg . esponja de platino
Preguntas y respuestas
P: ¿Qué es la lámpara de Döbereiner?
R: La lámpara de Döbereiner es uno de los primeros encendedores desarrollados en 1823 por el químico alemán Johann Wolfgang Döbereiner. Se fabricó hasta 1880 aproximadamente y aún puede verse en el Castillo de Heidelberg y en el Deutsches Museum (Museo Alemán).
P: ¿Cómo funciona?
R: El encendedor funciona basándose en una reacción química entre el hidrógeno y el oxígeno. En el cilindro de cristal se almacena ácido sulfúrico mientras que el zinc se almacena en una botella abierta en la parte superior con una válvula. Cuando se abre la palanca, el ácido sulfúrico fluye hacia la botella, lo que produce gas hidrógeno que pasa por el platino antes de reaccionar con el oxígeno del aire para producir agua como reacción exotérmica. Para detener esta reacción, es necesario soltar la palanca para que el hidrógeno ya no pueda salir de la botella y empuje de nuevo el ácido sulfúrico a su recipiente original.
P: ¿Quién inventó la lámpara de Döbereiner?
R: La lámpara de Döbereiner fue inventada por el químico alemán Johann Wolfgang Döbereiner en 1823.
P: ¿Dónde se pueden encontrar versiones originales de este encendedor?
R: Se pueden encontrar versiones originales de este encendedor en el Castillo de Heidelberg y en el Deutsches Museum (Museo Alemán).
P: ¿Qué elementos se utilizan para esta reacción química?
R: Esta reacción química utiliza como elementos hidrógeno, oxígeno, zinc, ácido sulfúrico, platino y agua.
P: ¿Qué ocurre cuando suelta la palanca?
R: Cuando suelta la palanca, impide que se produzcan más reacciones porque el hidrógeno ya no puede salir de la botella, lo que hace que el ácido sulfúrico vuelva a su recipiente original.
Buscar dentro de la enciclopedia

