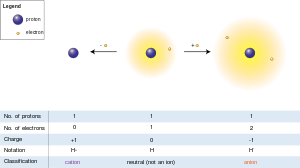
La IUPAC recomienda el uso de iones de hidrógeno como término general para todos los iones de hidrógeno y sus isótopos. Según la carga del ion, hay dos tipos: iones con carga positiva e iones con carga negativa.
Iones con carga positiva (H+ y sus variantes)
H+ representa el catión más simple: un protón desnudo. En fase gaseosa aislada puede existir como H+, pero en la mayoría de los entornos químicos reales —especialmente en soluciones acuosas— no se encuentra libre: se solvata fuertemente formando especies coordinadas con moléculas de solvente. En agua, la forma más estable y común es el ion hidronio, H3O+, aunque existen clústeres de hidratación como H5O2+ o H9O4+ dependiendo de la estructura de la red de agua.
- Concepto ácido–base: Según Brønsted–Lowry, un ácido dona H+ y una base lo acepta. La concentración efectiva de “protones” en solución acuosa se expresa mediante la escala de pH (pH = −log[H+]).
- Química de protonación: La transferencia de protones es una de las reacciones químicas más rápidas y fundamentales en química y bioquímica (enzimas, transporte de protones en membranas, catálisis ácida).
- Electroquímica y energía: Los protones participan en reacciones redox relevantes (por ejemplo, en pilas de combustible y en la reacción de evolución de hidrógeno).
Iones con carga negativa (H−, hidruro)
H− es el anión hidrudo: un ion hidrógeno con un electrón adicional. Presenta propiedades muy diferentes a H+:
- Basicidad y reactividad: H− es una base y un agente reductor fuerte; reacciona con protones para formar H2 y con electrófilos en síntesis orgánica (por ejemplo, reactivos como NaH o LiAlH4 entregan equivalentes de H−).
- Formación en sólidos: Muchos hidruros metálicos contienen H− enlazado a metales (hidruros alcalinos y alcalinotérreos, hidruros intersticiales en metales de transición, etc.).
- Estabilidad: En fase gaseosa puede detectarse H− en estudios espectroscópicos; en solución requiere medios no protónicos o bases fuertes para evitar la protonación inmediata.
Isótopos del hidrógeno y sus iones
El hidrógeno tiene tres isótopos naturales principales: protio (1H), deuterio (2H o D) y tritio (3H o T). Cada uno puede formar iones equivalentes:
- D+ (deuterón) y T+ (tritón) son los cationes análogos a H+. Tienen mayor masa y, en el caso del tritio, radioactividad beta.
- Los aniones D− y T− se comportan químicamente de forma parecida a H−, pero las diferencias de masa producen efectos isotópicos en las velocidades de reacción y en las propiedades vibracionales.
- Efectos isotópicos: Las diferencias de masa entre H, D y T generan efectos cinéticos e isotópicos (por ejemplo, enlaces D–X son generalmente más fuertes y reaccionan más lentamente que H–X), lo que se usa en estudio de mecanismos y en trazado isotópico.
Marcos conceptuales y nomenclatura
- Nomenclatura IUPAC: El término general recomendado es “iones de hidrógeno” para englobar todos los cationes y aniones derivados del hidrógeno y sus isótopos.
- Punto de vista Lewis: Un catión H+ actúa como ácido de Lewis (aceptor de pares de electrones) mientras que H− actúa como base de Lewis (donador de electrones).
Importancia práctica y aplicaciones
- Química orgánica: Hidruros (fuentes de H−) se usan ampliamente en reducciones (p. ej., LiAlH4, NaBH4) y en síntesis.
- Bioquímica y fisiología: Gradientes de protones (H+) son esenciales para la producción de ATP en mitocondrias y cloroplastos mediante síntesis por ATP sintasa.
- Industria energética: El manejo de protones y la generación de H2 son claves en tecnologías como pilas de combustible e hidrógeno como vector energético.
- Investigación: Los isótopos de hidrógeno se usan como trazadores (deuterio) y en estudios nucleares (tritio), y la química de iones de hidrógeno es fundamental en espectroscopía y catálisis.
Aspectos de seguridad y manipulación
- Los hidruros metálicos pueden ser reactivos y, en contacto con agua, liberar H2 y calor; algunos son pirofóricos.
- El tritio es radiactivo y requiere controles específicos de manipulación y dispoción.
- La liberación de H2 puede formar mezclas explosivas con aire; se deben seguir normas de ventilación y detección.
En resumen, “iones de hidrógeno” es un término amplio que incluye desde protones fuertemente solvata dos en solución acuosa (H+, H3O+) hasta aniones hidruro (H−) y sus equivalentes isotópicos (D+, T+, D−, T−). Su química gobierna fenómenos fundamentales en ácido‑base, catálisis, bioenergética y tecnología del hidrógeno.