Un microscopio de fluorescencia es un microscopio óptico que aprovecha la fluorescencia —y en algunos casos la fosforescencia— para visualizar y estudiar sustancias orgánicas e inorgánicas. Por "microscopio de fluorescencia" se entiende cualquier microscopio que utilice la emisión de luz inducida por excitación para formar una imagen, ya sea en un montaje sencillo o en un diseño avanzado con múltiples canales y detección sensible.
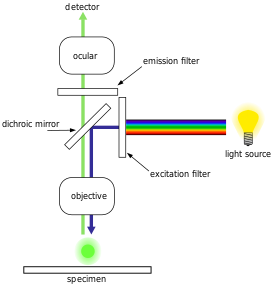
La mayoría de los microscopios de fluorescencia empleados en las ciencias de la vida usan el diseño de epifluorescencia. En este esquema la luz de la longitud de onda de excitación ilumina la muestra a través de la lente del objetivo. La fluorescencia emitida por el espécimen se recoge por el mismo objetivo y se dirige hacia el ocular o hacia un detector. Un divisor de haz dicroico (espejo dicrómico) y filtros de excitación/emitancia seleccionan las longitudes de onda: transmiten la luz de emisión al detector y reflejan o bloquean la luz de excitación residual hacia la fuente, mejorando el contraste de la imagen.
Componentes principales
- Fuente de excitación: lámparas de arco (Hg, Xe), lámparas de mercurio de baja presión, láseres o LEDs de alta potencia según la aplicación.
- Sistemas de filtrado: filtros de excitación, filtros de emisión y divisores dicroicos que separan las bandas espectrales.
- Objetivos de alta NA: objetivos corregidos para fluorescencia con alta apertura numérica para maximizar la recolección de fotones.
- Montura y portaobjetos: dispositivos de sujeción y etapas (manuales o motorizadas) para posicionar la muestra.
- Sensores y detectores: cámaras CCD, EM-CCD, sCMOS o detectores puntuales como PMT en microscopía confocal.
- Filtros multicanal y cubetas: para observación simultánea o secuencial de varios fluorocromos.
Principio de funcionamiento
Un fluoróforo absorbente en la muestra captura fotones de una longitud de onda específica (excitación) y, tras una corta vida excitada, emite fotones de menor energía (emisión) en una longitud de onda más larga. El microscopio excita selectivamente esos fluoróforos y recoge la luz de emisión mientras bloquea la luz de excitación, formando así una imagen con alto contraste de las regiones que contienen la señal fluorescente.
Tipos y variantes
- Epifluorescencia amplia (widefield): iluminación de todo el campo, adecuada para imágenes rápidas y muestras delgadas.
- Microscopía confocal: utiliza un pinhole para eliminar la luz fuera de foco y obtener mayor resolución axial y contraste en muestras tridimensionales.
- TIRF (Total Internal Reflection Fluorescence): excita sólo una capa muy fina cercana a la superficie, ideal para estudiar membranas y eventos en la interfaz célula-superficie.
- Microscopía de barrido láser y de disco confocal: para adquisición rápida de secciones ópticas y reconstrucción 3D.
- Técnicas de superresolución: STED, PALM, STORM y SIM permiten superar el límite de difracción y alcanzar resoluciones por debajo de 100 nm.
Preparación de la muestra y fluoróforos
Las muestras pueden marcarse con colorantes sintéticos (DAPI, FITC, TRITC), proteínas fluorescentes (GFP, mCherry) o sondas específicas (anticuerpos conjugados). Es importante controlar la autofluorescencia del sustrato, usar montajes anti-fotoblanqueo y, cuando procede, fijar y permeabilizar las células para permitir el acceso de sondas. La elección del fluoróforo debe considerar el espectro de excitación/emisión y la compatibilidad con los filtros del microscopio.
Aplicaciones
- Biología celular y molecular: localización de proteínas, seguimiento de orgánulos, dinámicas intracelulares.
- Histología y patología: diagnóstico mediante tinciones fluorescentes y multiplexadas.
- Microbiología: identificación de microorganismos, ensayos de viabilidad.
- Neurociencias: imagen funcional, trazado de circuitos y estudio de sinapsis.
- Biomedicina y diagnóstico clínico: citometría de imágenes, pruebas inmunofluorescentes.
- Ciencias de materiales y nanotecnología: caracterización de materiales fluorescentes y defectos.
Ventajas y limitaciones
- Ventajas: alta sensibilidad, gran contraste molecular, posibilidad de marcar múltiples dianas y observar procesos en tiempo real.
- Limitaciones: fotoblanqueo y fototoxicidad en muestras vivas, resolución limitada por la difracción (salvo técnicas de superresolución), posible autofluorescencia y necesidad de una correcta selección de filtros y fluoróforos.
Consideraciones prácticas y seguridad
Para obtener imágenes de calidad conviene usar objetivos de alta apertura numérica, calibrar y alinear el sistema de iluminación, y emplear montajes y soportes adecuados. Mantener limpios los filtros y el objetivo, y revisar regularmente la alineación óptica y el estado de las fuentes de luz y cámaras. En términos de seguridad, muchos sistemas de excitación usan luz intensa en el rango UV/azul: se deben seguir medidas de protección ocular y evitar la exposición directa.
En resumen, el microscopio de fluorescencia es una herramienta esencial en investigación y diagnóstico que permite visualizar con alta especificidad moléculas y estructuras en muestras biológicas y materiales, siempre que se controle la preparación de la muestra, la elección de fluoróforos y las limitaciones instrumentales.