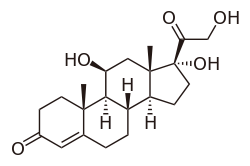
Los corticoesteroides son una clase de hormonas esteroides producidas en la corteza suprarrenal de los vertebrados. El término también se utiliza para los análogos sintéticos de estas hormonas.
Las dos clases principales de corticosteroides son los glucocorticoides y los mineralocorticoides. Realizan una amplia gama de procesos fisiológicos:
Funciones principales
- Glucocorticoides: regulan el metabolismo de carbohidratos, proteínas y lípidos; controlan la respuesta inflamatoria e inmune; participan en la respuesta al estrés (p. ej., el cortisol).
- Mineralocorticoides: regulan el equilibrio de sodio, potasio y agua, y por tanto la presión arterial (p. ej., la aldosterona).
- Ambas clases influyen en procesos como el desarrollo fetal (maduración pulmonar), el ritmo circadiano y la respuesta al trauma o infección.
Biosíntesis y regulación
Los corticoesteroides se sintetizan a partir del colesterol en la corteza suprarrenal. Su producción está regulada por el eje hipotálamo–hipófisis–suprarrenal (HHS): el hipotálamo libera CRH, la hipófisis secreta ACTH y esto estimula la síntesis de cortisol y otros esteroides. La liberación de glucocorticoides sigue un ritmo circadiano (picos matutinos) y aumenta ante estrés físico o emocional.
Mecanismo de acción
- Los glucocorticoides difunden a la célula y se unen a receptores citoplasmáticos (receptor de glucocorticoides, RGC). El complejo hormona‑receptor se transloca al núcleo y modula la transcripción génica: transactivación (aumento de la expresión de genes antiinflamatorios) y transrepresión (inhibición de genes proinflamatorios).
- Los mineralocorticoides actúan mediante el receptor mineralocorticoide (RMC) en células renales y otros tejidos; la enzima 11β‑HSD2 protege estos receptores degradando cortisol a cortisona, permitiendo que la aldosterona actúe específicamente.
Ejemplos clínicos y fármacos comunes
- Glucocorticoides naturales: cortisol (hidrocortisona).
- Glucocorticoides sintéticos: prednisona/prednisolona, metilprednisolona, dexametasona, betametasona. Varían en potencia, vida media y actividad mineralocorticoide.
- Mineralocorticoide sintético: fludrocortisona (utilizada en insuficiencia suprarrenal primaria para mantener el balance sodio-potasio y la presión arterial).
- Usos frecuentes: enfermedades inflamatorias y autoinmunes (artritis reumatoide, lupus), asma y EPOC, alergias severas, rechazo de trasplantes, tratamiento de insuficiencia suprarrenal (terapia de reemplazo), choque séptico en ciertos protocolos, y uso obstétrico (maduración pulmonar fetal en riesgo de parto prematuro).
Vías de administración
Oral, intravenosa, intramuscular, inhalada, tópica (corticoides dermatológicos), oftálmica, intraarticular y epidural. La vía se elige según la indicación y la necesidad de efecto sistémico versus local.
Efectos adversos y riesgos
El uso prolongado o en dosis altas puede producir efectos importantes:
- Supresión del sistema inmune y mayor riesgo de infecciones.
- Hiperglucemia y descompensación de diabetes.
- Osteoporosis y mayor riesgo de fracturas.
- Hipertensión, retención de sodio y edema (más marcado con actividad mineralocorticoide).
- Ganancia de peso, lipodistrofia (cara de luna), atrofia cutánea, estrías.
- Alteraciones psiquiátricas: insomnio, cambios de humor, euforia o depresión.
- Cataratas y glaucoma tras uso prolongado (especialmente con corticosteroides sistémicos u oftálmicos).
Supresión adrenal y pauta de retirada
La administración prolongada de glucocorticoides exógenos puede suprimir la producción endógena por inhibición del eje HHS. Por ello, al suspender tratamientos prolongados suele ser necesario disminuir la dosis progresivamente (tapering) para permitir la recuperación adrenal y evitar una insuficiencia suprarrenal aguda. La duración de terapia y la dosis determinan la necesidad y la velocidad de la reducción.
Interacciones y monitorización
Es importante monitorizar:
- Presión arterial, glucemia y electrolitos.
- Signos de infección y función ósea (densitometría en tratamientos crónicos).
- Ojo: examen oftalmológico si uso prolongado.
Interacciones farmacológicas relevantes incluyen potenciación de efectos hiperglucemiantes con algunos antidiabéticos, y cambios en el metabolismo de fármacos por CYP450 (p. ej., dexametasona puede alterar niveles de otros medicamentos).
Consideraciones especiales
- Embarazo: algunos glucocorticoides atraviesan la placenta (dexametasona, betametasona) y se usan para maduración pulmonar fetal; otros (prednisona) son mayoritariamente inactivados por la placenta y pueden ser preferidos para tratar a la madre cuando se requiere menor exposición fetal.
- Niños: el uso crónico puede afectar el crecimiento; se debe monitorizar y ajustar dosis.
- Pacientes con infecciones activas, úlceras gástricas no tratadas o diabetes requieren precaución y supervisión médica.
Resumen
Los corticoesteroides (glucocorticoides y mineralocorticoides) son hormonas vitales con múltiples funciones fisiológicas y amplias aplicaciones terapéuticas. Su uso es muy eficaz en numerosas enfermedades inflamatorias, autoinmunes y en insuficiencia suprarrenal, pero requiere atención a efectos adversos, interacciones y a la posible supresión del eje corticosuprarrenal. Ante dudas sobre indicación, dosis, duración o retirada, consulte con su médico o especialista.