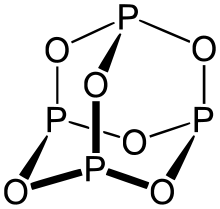
El óxido de fósforo (III), también conocido como trióxido de fósforo, es un compuesto químico. Su fórmula química es P2O3 (fórmula empírica) o P4O6 (fórmula molecular). Contiene fósforo en su estado de oxidación +3.
Estructura y naturaleza química
Contrario a la idea de que contiene iones separados de fósforo y de óxido, el trióxido de fósforo es un sólido molecular covalente formado por moléculas discretas de P4O6. La estructura puede describirse como una jaula derivada de la tetraedría P4, en la que las seis aristas están puenteadas por átomos de oxígeno, de modo que cada fósforo está enlazado a tres oxígenos (y cada oxígeno a dos fósforos). La molécula tiene simetría tetraédrica aproximada y es estable en ausencia de humedad y oxígeno en exceso.
Propiedades físicas
- Aspecto: sólido blanco a incoloro, a veces ceroso o cristalino.
- Volatilidad: es relativamente poco volátil pero puede sublimarse y es sensible a la oxidación en el aire.
- Solubilidad: reacciona con agua (no es estable en agua); puede disolverse en algunos disolventes orgánicos no polares.
- Estado de oxidación del fósforo: +3 en la molécula.
Propiedades químicas y reacciones importantes
- Hidrólisis: reacciona con agua para formar ácido fosforoso (H3PO3), con liberación de calor. Esta reacción hace que no sea estable en presencia de humedad:
P4O6 + 6 H2O → 4 H3PO3. - Oxidación: al oxidarse en exceso de oxígeno se transforma en P4O10 (óxido de fósforo (V) o pentóxido de fósforo).
- Formación de fosfitos: reacciona con alcoholes para dar ésteres fosfíticos (fosfitos), que son compuestos útiles en síntesis orgánica y como estabilizantes:
P4O6 + 12 ROH → 4 P(OR)3 + 6 H2O (reacción general, dependiendo de las condiciones). - Agente reductor: en ciertos contextos el fósforo en estado +3 puede comportarse como agente reductor frente a agentes más electronegativos.
Obtención
Se obtiene principalmente por la oxidación controlada del fósforo blanco en una cantidad limitada de oxígeno, deteniendo la reacción antes de que se forme el óxido más oxidado P4O10. En el laboratorio se prepara dejando arder fósforo blanco en una corriente de oxígeno diluida o mediante rutas sintéticas que implican la deshidratación parcial de especies fosforosas.
Usos
- Reactivo en síntesis química: precursor en la preparación de fosfitos (P(OR)3), útiles en síntesis orgánica y como ligandos en catálisis.
- Intermedio para la obtención de otros compuestos de fósforo en estado +3.
- Aplicaciones industriales limitadas comparadas con P4O10, pero importante en la química fina y en investigación.
Seguridad y manipulación
- El trióxido de fósforo es irritante y tóxico: puede provocar daño por inhalación, ingestión o contacto con la piel y ojos.
- Reacciona con agua liberando ácidos, por lo que debe manipularse bajo atmósfera seca, con guantes, gafas de protección y en campana de extracción si hay polvo o vapores.
- Se debe almacenar en recipientes bien cerrados, secos y, preferiblemente, bajo atmósfera inerte (nitrógeno o argón) para evitar su oxidación y su hidrólisis.
Nomenclatura y relación con otros óxidos de fósforo
El nombre sistema es óxido de fósforo(III) o fósforo(III) óxido; “trióxido de fósforo” es un nombre tradicional. Su fórmula empírica P2O3 refleja la relación estequiométrica, mientras que P4O6 indica la unidad molecular real. Está relacionado con otros óxidos del fósforo como el pentóxido (P4O10), que contiene fósforo en estado +5 y es muy más oxidante y desecante.
En resumen, el trióxido de fósforo (P4O6) es un compuesto molecular de fósforo en estado +3 con una estructura en jaula, útil como precursor de fosfitos y como reactivo en química, pero requiere medidas de seguridad por su reactividad con agua y su toxicidad.