La calorimetría diferencial de barrido (DSC) es una técnica analítica termal ampliamente utilizada en las ciencias de los materiales, la termoquímica, el control de la pureza y la formulación de fármacos, así como en el aseguramiento de la calidad de alimentos y otros productos. El DSC mide cómo varía el flujo de calor hacia o desde una muestra con respecto a una referencia bien definida cuando se somete a un programa de temperatura controlado. Esta información permite identificar y cuantificar transiciones térmicas (por ejemplo, transición vítrea, fusión, cristalización, curado o desnaturalización), determinar entalpías y capacidades caloríficas, y estudiar cinéticas de reacciones térmicas. El DSC fue ideado por E.S. Watson y M.J. O'Neil en 1962 y presentado comercialmente por primera vez en 1963 en la conferencia de Química Analítica y Espectroscopia Aplicada celebrada en Pittsburgh.
Estructura física y principio de funcionamiento
Existen dos diseños básicos de DSC:
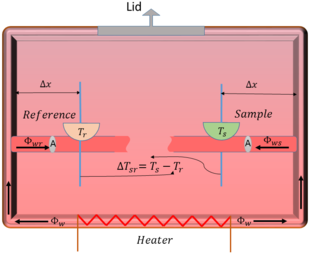
- DSC de flujo de calor: mantiene aproximadamente común la potencia suministrada al horno y mide la diferencia de temperatura entre el porta-muestras (con la muestra) y el porta-referencia (vacío o material inerte). La diferencia de temperatura se relaciona con la diferencia en flujo de calor.
- DSC de potencia compensada: mantiene constante la diferencia de temperatura entre muestra y referencia compensando la potencia eléctrica; la señal medida es la potencia necesaria para mantener esa igualdad térmica.
El diseño típico incluye: porta-muestras y porta-referencia (pequeños cráneos o cápsulas metálicas), un horno o baño calefactor con resistencia, termopares para medir la temperatura en cada celda y un sistema de control y registro. El calor fluye desde la resistencia hacia las cámaras de muestra y referencia; las pequeñas diferencias en flujo o potencia se registran como la señal DSC.
En muchos textos y equipos se hace referencia a una figura 1 que ilustra el montaje (horno, soportes, termopares y crucetas). Además de los diseños estándar, existen variantes modernas (por ejemplo, DSC modulada, micro-DSC o DSC de alta velocidad) que amplían las capacidades de análisis.
Eventos térmicos que puede detectar el DSC
- Transición vítrea (Tg): cambio en la capacidad calorífica sin liberación o absorción neta de calor latente.
- Fusión (melting): pico endotérmico con entalpía de fusión asociada.
- Cristalización: pico exotérmico si la muestra cristaliza al enfriarse o calentarse.
- Curado o reticulación de polímeros: picos exotérmicos que permiten cuantificar la entalpía de curado y el grado de conversión.
- Transiciones de fase y polimorfismo: cambios en la estructura cristalina o transiciones sólido–sólido.
- Desnaturalización de proteínas y fusión de biopolímeros: picos endotérmicos característicos.
- Oxidación o índices de estabilidad (OIT, OOT): determinación de la resistencia a la oxidación bajo atmósferas específicas.
- Medida de capacidad calorífica (Cp) y análisis termodinámico cuantitativo.
Interpretación de la señal y parámetros clave
Los parámetros principales que se extraen de un termograma DSC son:
- Temperatura de inicio u onset: punto donde comienza la desviación respecto de la línea base; útil para comparar temperaturas de transición.
- Temperatura de pico: máxima señal del evento (ej. máximo de fusión o desnaturalización).
- Área bajo el pico: integrada en unidades de energía (J) y, dividida por la masa de muestra, da la entalpía específica (J/g) del evento.
- Cambio en Cp: magnitud del salto en la línea base en la Tg, relacionado con la capacidad calorífica.
- Forma y ancho del pico: proporcionan información sobre la cinética del proceso y la heterogeneidad de la muestra.
Para obtener valores precisos se requiere una calibración periódica (por ejemplo usando materiales estándares como indio para entalpías y punto de fusión, y zafiro para Cp) y una corrección de línea base. La cinética aparente del proceso depende fuertemente de la velocidad de calentamiento; diferentes velocidades desplazan los onsets y picos.
Modos y variantes instrumentales
- DSC modulada (MDSC): superpone una pequeña oscilación de temperatura sobre la rampa media, permitiendo separar el flujo de calor reversible (asociado a Cp) del no reversible (cinéticos, crystallización rápida, curado).
- Fast DSC o micro-DSC: permite tasas de calentamiento/enfriamiento muy altas para estudiar procesos rápidos o simular condiciones reales de procesamiento.
- DSC de alta presión o con atmósfera controlada: permite trabajar con gases reactivos o presiones elevadas para estudiar oxidación u otras reacciones en condiciones específicas.
Preparación de muestras y condiciones experimentales
- Masa típica: desde microgramos a decenas de miligramos, dependiendo del equipo y sensibilidad.
- Tipo de cápsulas o crisol: aluminio (común), acero inoxidable, crisol hermético o sellado para muestras volátiles y sensibles al oxígeno.
- Atmósfera: nitrógeno o argón para condiciones inertes; aire o oxígeno para estudios de oxidación.
- Velocidad de calentamiento/enfriamiento: valores típicos 1–20 °C/min, aunque se emplean tasas mayores o menores según el objetivo. La elección influye en la resolución y la cinética aparente.
- Sellado adecuado para evitar pérdida de volátiles o reacciones con el ambiente; limpieza y homogeneidad de la muestra son críticas.
Aplicaciones prácticas
- Polímeros: determinación de Tg, entalpía de fusión y cristalización, grado de curado, estabilidad térmica y compatibilidad entre fases.
- Farmacéutica: identificación de formas polimórficas, estudios de estabilidad, determinación de pureza (método de Van’t Hoff aproximado mediante entalpía de fusión), y compatibilidad excipiente-fármaco.
- Alimentos: caracterización de grasas y aceites (perfil de fusión), evaluaciones de calidad y estabilidad, y análisis de procesos de cristalización.
- Biociencias: estudios de desnaturalización proteica, interacciones ligando-proteína y estabilidad de formulaciones biológicas (con micro-DSC o DSC de bajas masas).
- Materiales avanzados y metales: identificación de transiciones de fase, determinación de temperaturas críticas y estudios termodinámicos en aleaciones y cerámicos.
- Control de calidad y regulación: comprobación de lotes, especificaciones de proceso y garantía de reproducibilidad en fabricación.
Ventajas y limitaciones
- Ventajas: técnica rápida, relativamente sencilla de usar, proporciona información cuantitativa sobre entalpías y Cp, y es aplicable a un amplio rango de materiales.
- Limitaciones: no aporta información estructural directa (se complementa con técnicas como DSC + XRD o espectroscopía), la señal depende de la calidad del contacto térmico y del tamaño de muestra, y la interpretación puede verse afectada por eventos superpuestos y por la dependencia de la velocidad de calentamiento.
Calibración, control de calidad y seguridad
La calibración regular con estándares (indio, zinc, zafiro) y la verificación de la línea base son necesarias para resultados fiables. Es importante registrar condiciones experimentales completas (masa, tipo de crisol, atmósfera, velocidad) para poder reproducir y comparar datos. En cuanto a seguridad, manejar con cuidado los crisolados tras ensayos a alta temperatura, vigilar gases empleados y evitar sobrepresiones en cápsulas selladas.
En resumen, el DSC es una técnica esencial en el análisis térmico, capaz de ofrecer datos termodinámicos y cinéticos valiosos para investigación y control de calidad en múltiples industrias; su correcta aplicación requiere una buena preparación de muestras, calibración y entendimiento de las limitaciones instrumentales.