La ley de Boyle (también llamada ley de Mariotte y ley de Boyle-Mariotte) es una ley sobre los gases ideales que describe la relación entre la presión y el volumen de una cantidad fija de gas cuando la temperatura permanece constante.
La ley puede enunciarse de forma concisa:
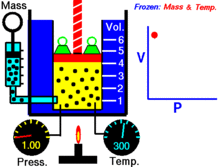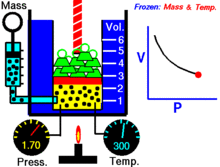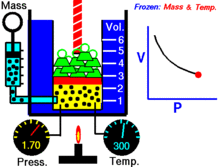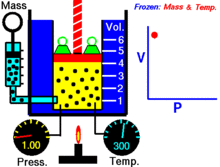
Para una cantidad fija de un gas ideal mantenido a una temperatura fija, P (presión) y V (volumen) son inversamente proporcionales.
Fórmula y expresión matemática
En símbolos, la proporcionalidad se escribe:
P ∝ 1 V {\displaystyle P\propto {\frac {1}{V}}
O bien, multiplicando ambos miembros por V, se obtiene que el producto presión·volumen es constante:
P V = k {\displaystyle PV=k}
donde P es la presión del gas, V el volumen ocupado por el gas y k una constante que depende de la cantidad de gas y de la temperatura. Para una masa fija de gas a temperatura constante, el producto PV permanece constante: cuando el volumen disminuye, la presión aumenta proporcionalmente, y viceversa.
Forma práctica: estados inicial y final
Si conocemos las condiciones iniciales (P1, V1) y cambiamos a unas condiciones finales (P2, V2), la constante k toma el mismo valor en ambos estados, por lo que:
P 1 V 1 = k {\displaystyle P_{1}V_{1}=k}
P 2 V 2 = k {\displaystyle P_{2}V_{2}=k}
De donde se obtiene la relación utilizada con frecuencia:
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}
Ejemplo resuelto
Ejemplo: La presión de un gas es de 3 atm y su volumen es de 5 litros. Si la presión se reduce a 2 atm, ¿cuál será el volumen?
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}
Despejando V2:
V 2 = P 1 V 1 P 2 {\displaystyle V_{2}={\frac {P_{1}V_{1}}{P_{2}}}}
Sustituyendo: V2 = (3 atm · 5 L) / 2 atm = 15 / 2 L = 7,5 L.
V 2 = 3 ∗ 5 2 {\displaystyle V_{2}={\frac {3*5}}
V 2 = 15 2 {\displaystyle V_{2}={frac {15}{2}}
V 2 = 7,5 {\displaystyle V_{2}=7,5}
∴ El volumen será de 7,5 litros.
Explicación microscópica (intuición física)
Desde la teoría cinética de los gases, la presión resulta de las colisiones de las moléculas del gas contra las paredes del recipiente. Al reducir el volumen manteniendo constante el número de moléculas y la temperatura (energía cinética promedio), las colisiones por unidad de área y por unidad de tiempo aumentan, y por tanto aumenta la presión. Esa es la razón física de la proporcionalidad inversa entre P y V.
Condiciones de validez y limitaciones
- La ley de Boyle se cumple para gases ideales o cuando las interacciones entre moléculas son despreciables. En la práctica, es una buena aproximación a bajas densidades (presiones moderadas) y temperaturas lejos de la condensación.
- No se aplica si la temperatura varía; en ese caso hay que usar la ley general de los gases (PV = nRT) o las relaciones correspondientes entre P, V y T.
- Para gases reales a alta presión o cerca del punto de licuefacción, las desviaciones son apreciables y se usan ecuaciones de estado más generales (por ejemplo, la ecuación de van der Waals).
Relación con la ecuación de estado de los gases ideales
La ley de Boyle se obtiene directamente de la ecuación de los gases ideales:
PV = nRT
Si la cantidad de sustancia n y la temperatura T son constantes, entonces PV = (nR T) = constante, lo que da lugar a la ley de Boyle.
Representación gráfica y trabajo en un proceso isotérmico
- En un gráfico P versus V, la ley de Boyle se representa por una hipérbola equidimensional (P = k/V).
- En un proceso isotérmico reversible del gas ideal, el trabajo realizado por el gas al expandirse de V1 a V2 es: W = ∫V1V2 P dV = nRT ln(V2/V1)(esto usa PV = nRT constante de estado isotérmico).
Aplicaciones prácticas
- Jeringas y pistones: al empujar el pistón se reduce el volumen y aumenta la presión del gas dentro.
- Dispositivos de buceo y cámaras hiperbáricas: comprensión del comportamiento P–V en procesos de compresión/expansión
- Ingeniería de procesos y compresores: dimensionado y control de equipos que comprimen gases.
- Instrumentación: algunos manómetros y sistemas neumáticos se diseñan teniendo en cuenta relaciones P–V.
Historia
La ley fue encontrada por Robert Boyle en 1662 mediante experimentos con tubos y pistones; de forma independiente, Edme Mariotte la formuló en 1679. Por eso a veces se la denomina ley de Boyle-Mariotte.
En resumen, la ley de Boyle establece que, para una masa fija de gas ideal a temperatura constante, la presión y el volumen son inversamente proporcionales y su producto es constante (PV = constante). Esta relación es una de las leyes fundamentales que describen el comportamiento macroscópico de los gases y se deriva directamente de la ecuación de estado de los gases ideales cuando n y T permanecen constantes.