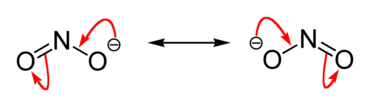
El nitrito es un ion. Su fórmula química es NO2–. Contiene nitrógeno en su estado de oxidación +3. Los nitritos son normalmente fuertes agentes oxidantes. La mayoría de ellos son compuestos cristalinos incoloros. El nitrito de sodio es un nitrito común. También son agentes reductores débiles, que se oxidan a nitratos (NO3–).
Estructura y propiedades químicas
El ion nitrito, NO2–, es plano y presenta resonancia. Sus dos enlaces N–O son equivalentes por resonancia, con un orden de enlace aproximado de 1,5, lo que da longitudes de enlace intermedias entre un enlace simple y uno doble. El átomo de nitrógeno tiene hibridación sp2, y la geometría efectiva alrededor del nitrógeno es angular (doblete de electrones no compartidos en el nitrógeno que provoca el doblamiento), con un ángulo O–N–O cercano a 115–120°.
Químicamente, el nitrito es anfótero en reacciones redox: puede actuar como agente oxidante (por ejemplo, oxidándose en ciertos sustratos orgánicos o en presencia de agentes reductores) o como agente reductor (si se encuentra con oxidantes más fuertes), dependiendo del pH y del medio. En medios ácidos el nitrito suele reducirse a óxidos de nitrógeno (NO, N2O, etc.), mientras que en condiciones oxidantes puede transformarse a nitrato (NO3–).
Obtención y reacciones importantes
Los nitritos se obtienen industrialmente y en laboratorio por varias vías: reducción parcial de nitratos, disolución de óxidos de nitrógeno en agua seguida de reacciones controladas, y como productos intermedios en los procesos biológicos del ciclo del nitrógeno (nitrificación y desnitrificación bacteriana). Las sales de nitrito, como el nitrito de sodio (NaNO2), son muy solubles en agua y se aíslan con facilidad.
Reacciones típicas:
- Oxidación a nitrato: el nitrito puede oxidarse a NO3– en presencia de oxidantes fuertes o por exposición al oxígeno en ciertas condiciones.
- Reducción a óxidos de nitrógeno: en medios ácidos puede formarse monóxido de nitrógeno (NO) u otros óxidos de nitrógeno.
- Formación de diazonio en química orgánica: el ion nitrito se emplea para generar especies nitrosantes (NO+) que reaccionan con aminas primarias aromáticas formando sales diazonio, reacción básica en la síntesis de colorantes y en la química analítica.
Usos
Los nitritos y sus sales tienen múltiples aplicaciones:
- Conservación y curado de alimentos: El nitrito de sodio y otros nitritos se emplean en el curado de carnes para estabilizar el color (dan el color rosado característico), inhibir el crecimiento de bacterias como Clostridium botulinum y mejorar el sabor. Debido a la formación potencial de nitrosaminas cancerígenas, su uso y dosis están regulados.
- Antídotos médicos: El nitrito de sodio se utiliza, en combinación con otros compuestos (por ejemplo, tiosulfato), como antídoto en intoxicaciones por cianuro; induce methemoglobinemia parcial que ayuda a secuestrar el cianuro.
- Industria química: Empleado en la síntesis de colorantes, productos farmacéuticos y como reactivo nitrosante en diversas transformaciones orgánicas.
- Tratamiento del agua y control industrial: Uso en inhibidores de corrosión, en procesos de laboratorio y en la elaboración de productos intermedios.
- Analítica: El ion nitrito se determina mediante técnicas como la reacción de Griess (formación de un azocompuesto coloreado), cromatografía iónica o espectrofotometría.
Riesgos para la salud y el medio ambiente
El nitrito es tóxico en concentraciones elevadas. Puede provocar metahemoglobinemia, una condición en la que la hemoglobina no puede transportar oxígeno eficientemente; los lactantes son especialmente sensibles (síndrome del “bebé azul”). Además, en condiciones ácidas y en presencia de aminas secundarias o aminas terciarias el nitrito puede formar nitrosaminas, compuestos potencialmente cancerígenos.
Por estas razones, organismos reguladores monitorizan y limitan las concentraciones de nitrito en agua potable y alimentos. La exposición ambiental a través de aguas contaminadas por fertilizantes, aguas residuales o descargas industriales es una preocupación, ya que puede afectar tanto a la salud humana como a ecosistemas acuáticos.
Análisis y control
La cuantificación de nitrito en muestras ambientales, alimentarias o biológicas se realiza mediante:
- Reacción de Griess (colorimetría) — método rápido y ampliamente usado.
- Cromatografía iónica — para determinaciones precisas en matrices complejas.
- Espectroscopía y métodos electroquímicos — en aplicaciones especializadas.
Las medidas de control incluyen tratamiento de aguas residuales, manejo adecuado de fertilizantes, y regulaciones sobre niveles máximos permitidos en alimentos y agua potable para reducir riesgos sanitarios.
Ejemplos y seguridad
El nitrito de sodio (NaNO2) y el nitrito de potasio (KNO2) son sales comunes comercialmente disponibles. Aunque útiles en muchas aplicaciones, deben manejarse con precaución: usar protección personal, evitar la ingestión y seguir las normativas locales sobre almacenamiento y eliminación.
Resumen: El ion nitrito (NO2–) es un anión clave en química y en el ciclo del nitrógeno, con propiedades de resonancia y comportamiento redox versátil. Tiene aplicaciones industriales y alimentarias importantes, pero su toxicidad y la potencial formación de compuestos nocivos requieren un manejo y control adecuados.